
| Rome University, La Sapienza Chemistry Department Rome, Italy, Europe |
Dr. Giovanni Visco Cenni di statistica di base. Calcoli di regressioni e correlazioni. novembre 2005 |
Corso di Laurea in Scienze Applicate ai Beni Culturali ed alla Diagnostica per la loro Conservazione |
| previous slide, 6 | next slide, 8 |
Ancora una volta prima di studiare la regressione dobbiamo analizzare uno strumento di misura, lo spettrofotometro, per capire da dove provengono i dati che utilizzeremo.
Un'altra equazione su cui e' stata costruita una metodica analitica importantissima e' quella di Beer-Lambert-Bouguer. Data una soluzione che assorbe luce (UV o Visibile) ad una data lunghezza d'onda questa legge fornisce una relazione, lineare, fra concentrazione ed assorbimento.
Iniziamo con un bel disegno (preso da un sito Internet ma pesantemente modificato) che mostra con semplicita' la struttura di uno spettrofotometro, doppio raggio, che sfrutta la legge di Lambert-Beer.

Iniziando da destra verso sinistra descriviamo i singoli componenti:
Studiamo l'assorbimento allo spettrofotometro di un colorante industriale a varie concentrazioni via via decrescenti. L'assorbimento dovrebbe presentare un picco intorno ai 600 nm. Al variare della concentrazione troveremo lo stesso andamento visto per l'elettrodo.
Per le concentrazioni troppo elevate l'assorbimento di luce del campione e' cosi' forte che il meter non legge niente, per tutta una serie di concentrazioni ci sara' una lettura proporzionale, per le concentrazioni troppo basse la luce passa in modo uguale nel Blank e nel Sample e leggiamo solo rumore casuale.
Iniziamo dalle concentrazioni piu' elevate. Usando cuvette con cammino ottico di 10 mm ed uno spettrofotometro Perkin Elmer Lambda 15 otteniamo la sequenza di spettri qui sotto. Si nota che con alcune concentrazioni lo spettrofotometro sembra impazzire, saltano fuori impensabili difetti. Diminuendo la concentrazione gli spettri si sovrappongono e possiamo misurarne l'altezza del picco caratteristico che e' (dovrebbe essere) funzione della concentrazione. Questo e' lo spettro in uscita dal registratore (AcidBlue1.png, 61KBytes), usate il pulsante back per tornare qui.
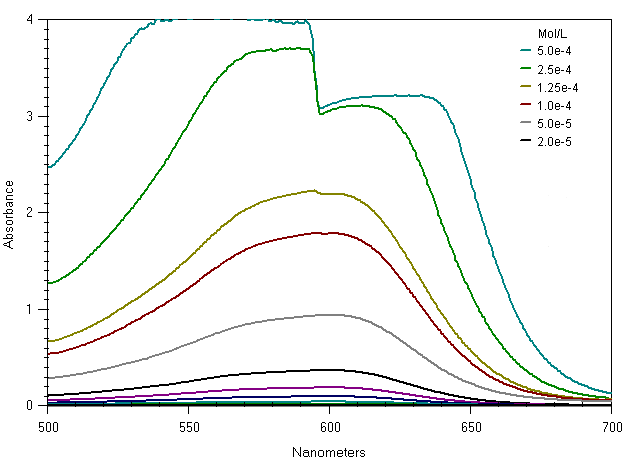
Un valore limite (con questo analita, con queste cuvette, con questo strumento) sembra essere la concentrazione 1.25 x 10-4 Mol/L. Si nota che gia' con questa concentrazione la soluzione ha un'assorbanza di 2 e che si produce ancora un difetto nello spettro (forse al cambio del rivelatore). Ricordiamo che dalla formula dell'assorbanza il valore 2 equivale ad una trasmittanza del solo 1%.
Con le concentrazioni intermedie gli spettri, qui sotto mostrati, non evidenziano deformazioni anomale e si possono con facilita' calcolare le altezze dei picchi di assorbimento. Qui potete vedere lo spettro in uscita dal registratore (AcidBlue2.png, 35KBytes), usate il pulsante back per tornare qui.
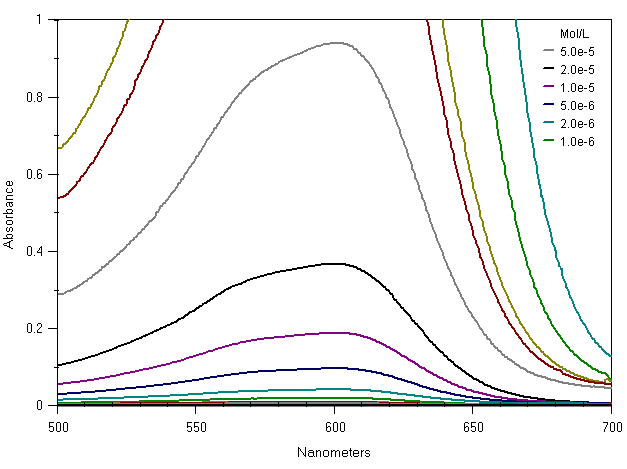
Questa e' di norma la zona tipica di utilizzo di uno spettrofotometro. Se le soluzioni sono troppo colorate o troppo diluite si puo' rientrare in questa zona scegliendo cuvette con cammino ottico da 1 mm fino a 100 mm.
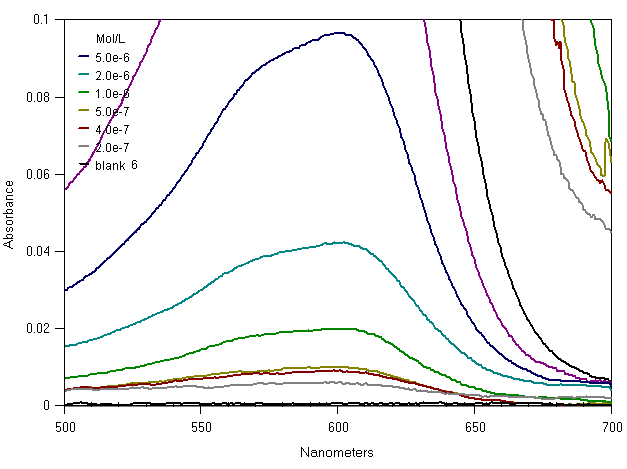
Ora siamo arrivati a concentrazioni cosi' basse che quasi non si riesce piu' a misurare l'altezza dello spettro. E' consigliabile guardare direttamente la sequenza di spettri a bassa concentrazione cosi' come esce dal registratore (AcidBlue3.png, 34KBytes, usate il pulsante back per tornare qui), si nota il rumore dovuto al forte flusso luminoso non assorbito ne' dal sample ne' dal blank.
Ora per ognuno degli spettri possiamo misurare il valore dell'assorbanza al valore massimo del picco, a circa 600 nanometri. Valori che riportiamo nella tabella qui sotto.
| Conc. Mol/L | 2.00 x 10-7 | 4.00 x 10-7 | 5.00 x 10-7 | 1.00 x 10-6 | 2.00 x 10-6 | 5.00 x 10-6 | 1.00 x 10-5 | 2.00 x 10-5 | 3.00 x 10-5 | 5.00 x 10-5 | 7.00 x 10-5 | 1.00 x 10-4 | 1.25 x 10-4 | 2.50 x 10-4 | 5.00 x 10-4 |
| Absorbance | 0.007 | 0.009 | 0.010 | 0.020 | 0.039 | 0.097 | 0.185 | 0.344 | 0.544 | 0.899 | 1.244 | 1.743 | 2.193 | 3.080 | 3.190 |
| Lambda max, nm | 597.5 | 598.5 | 600.0 | 601.0 | 599.5 | 599.0 | 601.0 | 601.5 | 601.0 | 601.5 | 601.0 | 602.0 | 602.5 | 611.5 | 623.5 |
Possiamo ora a disegnare il solito grafico concentrazione sull'asse X e l'altezza del picco (assorbanza) sull'asse Y.

Praticamente un grafico inutile, non si vedono le concentrazioni piu' basse, le uniche rappresentate sono quelle di mancata linearita' ad alti valori di assorbanza. Non si finisce mai di raccomandare che i grafici devono essere esplicativi e bisogna spendere una gran quantita' di tempo per far mostrare davvero al grafico quello che volevamo mostrare.
Le nostre misure si estendono per piu' di 3 unita' di concentrazione (o per meglio dire per 3 decadi e/o 3 ordini di grandezza). Il grafico deve evidenziare allo stesso modo sia le concentrazioni piu' elevate sia le concentrazioni piu' basse. Uno dei migliori esempi di grafico e' quello bi-logaritmico in cui ambedue le scale sono state convertite per mezzo della funzione X=log(x).
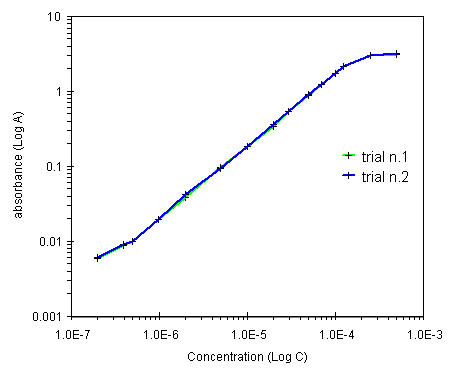
Nel grafico, con il solo colpo d'occhio, si puo' riconoscere una zona centrale (lineare ?), una zona di saturazione alle concentrazioni elevate, ed una zona di mancata risposta dello strumento alle concentrazioni piu' basse.
Molte, moltissime curve di risposta alle concentrazioni degli analiti sono come quella qui riportata. Analizzeremo questa curva con la regressione.
| previous slide | next slide |